Паучий шёлк прочнее стали в 5 раз: секрет раскрыт
Авторы: Gregory P. Holland, Christian D. Lorenz, Hannah R. Johnson, Kevin Chalek

Паутинная нить по удельной прочности превосходит сталь, а по вязкости разрушения — кевлар более чем в три раза (около 180 МДж/м³ против 50 МДж/м³), но долгое время оставалось совершенно непонятно, как именно пауку удается за доли секунды превратить жидкий «бульон» из белков в одну из самых надежных нитей на планете. Теперь исследователи наконец разгадали этот биохимический фокус — и это открытие может навсегда изменить современное производство материалов.
Исторический контекст
Паучий шелк — биоразлагаемый, лёгкий и феноменально прочный. Инженеры хотят использовать его для медицинских имплантатов, сверхпрочных бронежилетов, тросов подвесных мостов — везде, где нужна прочность при минимальном весе.
Однако все попытки массового производства искусственного паучьего шелка терпели неудачу. Разводить пауков на фермах, как тутовых шелкопрядов, невозможно — пауки территориальны и склонны к каннибализму. Синтезировать белки (спидроины) в лаборатории с помощью бактерий ученые научились, но при попытке вытянуть из них нить получался хрупкий и слабый материал. Проблема крылась не в составе «сиропа», а в самом механизме его кристаллизации. Ученым не хватало понимания, что именно запускает этот процесс на молекулярном уровне.
В 2018 году лаборатория Грегори Холланда в Университете штата Сан-Диего (SDSU) впервые объяснила, как пауки безопасно хранят шелковые белки в железах, не допуская преждевременной агрегации. Но вопрос оставался: что именно запускает переход из жидкости в твердое волокно?
Что открыли
Международная команда во главе с профессором Грегори Холландом (San Diego State University) и профессором Кристианом Лоренцем (Королевский колледж Лондона) наконец вычислила «недостающее звено». Оказалось, что «волшебной кнопкой», активирующей затвердевание, является обычный неорганический ион — фосфат.
Результаты опубликованы 22 декабря 2025 года в журнале Proceedings of the National Academy of Sciences (PNAS, том 122, выпуск 52, DOI: 10.1073/pnas.2523198122). Исследование финансировалось ВВС США (AFOSR), что отражает стратегический интерес к материалам будущего.
Катион-π взаимодействия (Cation-π interactions) Уникальный тип нековалентных, но очень сильных химических связей. Положительно заряженная гуанидиниевая группа аргинина притягивается к богатому электронами бензольному кольцу тирозина, скрепляя молекулы как мощная супер-застежка «липучка».
Исследователи установили, что именно добавление фосфата вытесняет воду вокруг шелковых белков, критически снижая их растворимость. Фосфат выступает в роли триггера, который заставляет аминокислоты аргинин и тирозин находить друг друга и объединяться через катион–π взаимодействия.

Как это работает
Для своего открытия команда использовала комбинацию передовых методов: моделирование структуры белков с помощью AlphaFold3, молекулярно-динамические симуляции и ЯМР-спектроскопию (ядерный магнитный резонанс).
На раннем этапе формирования шелка, когда раствор движется по каналу железы паука, происходит концентрация фосфата. Ионы фосфата вытесняют молекулы воды, убирая «гидратационный барьер» между белками. Белки образуют капли, подвергаясь фазовому разделению — они отделяются от воды подобно каплям масла. В этот момент аргинин и тирозин «защелкиваются» друг с другом.
Затем, когда паук механически вытягивает нить, эти микро-капли с застегнутыми химическими связями организуются в вытянутую, плотную β-слоистую структуру. Критически важно: аргинин частично встраивается в кристаллические регионы (β-листы), а тирозин формирует β-повороты на границах между упорядоченными и аморфными участками. Так создается наноструктурный композит, придающий волокну одновременно жесткость и эластичность.
Почему это меняет всё
Знание того, как активировать этот процесс с помощью простого фосфатного буфера, открывает прямую дорогу к масштабируемому промышленному синтезу паучьего шелка. Теперь в реакторах можно создавать жидкие спидроины, а затем, контролируемо меняя химическую среду (добавляя фосфат), производить волокно методом искусственного прядения.
Сверхлёгкая авиационная обшивка, экологичные аналоги пластика, биосовместимые хирургические нити — всё это переходит из разряда «интересный лабораторный эксперимент» в «реальный продукт». Рынок синтетического паучьего шелка уже оценивается в $12,4 млрд и, по прогнозам, достигнет $20 млрд к 2035 году.
Удивительно, но биохимия этого процесса имеет параллели с нейродегенеративными заболеваниями. Формирование амилоидных бляшек при болезни Альцгеймера происходит через похожее фазовое разделение белков — те же катион-π взаимодействия обнаружены и в рецепторах нейромедиаторов человека. Однако если паук эволюционно отточил контроль над этим процессом, то в мозге он идет «вразнос». Изучение пауков может дать ключ к пониманию и лечению болезней мозга.
Критический взгляд
Статья прошла рецензирование и опубликована в PNAS (декабрь 2025).
Особую убедительность исследованию придает методологическая строгость, скрывающаяся за обманчиво простым ответом. Идентификация фосфата как молекулярного триггера — это не предположение, а вывод, к которому независимо пришли три совершенно разных подхода: предсказание структуры белков с помощью AlphaFold3, молекулярно-динамические симуляции и ЯМР-спектроскопия. Когда три метода указывают на один механизм, это максимально близко к научной достоверности на данном масштабе. Работа при этом не возникает из ниоткуда: она прямо развивает открытие Холланда 2018 года о хранении белков в железах паука, окончательно замыкая цепочку, которая десятилетиями не давала покоя материаловедам. А область применения простирается далеко за пределы текстиля — те же катион-π взаимодействия, обнаруженные здесь, фигурируют в путях агрегации амилоидных белков, намекая, что биология паука может пролить свет на механизмы нейродегенеративных заболеваний.
Вместе с тем между знанием триггера и промышленным управлением им — огромная разница. Прядильный канал паука — это удивительно точное микрофлюидное устройство, поддерживающее тонко выверенные градиенты давления, pH и концентрации ионов по всей своей длине, и ни одна искусственная фильера пока убедительно их не воспроизвела. Понимание того, что фосфат инициирует фазовое разделение, — необходимое условие для синтеза шелка, но отнюдь не достаточное. Экономическая целесообразность масштабирования фосфат-индуцируемого синтеза от лабораторного реактора до коммерчески конкурентного производства остается полностью недоказанной.
Главный открытый вопрос, таким образом, лежит в области инженерии, а не биохимии: насколько точно нужно контролировать скорость и пространственный градиент концентрации фосфата в искусственных фильерах, чтобы получать нити со стабильными механическими свойствами в промышленном масштабе? Молекулярная инструкция наконец расшифрована. Создание машины, которая ей следует, — это уже следующая глава.
Что дальше
Следующий рубеж — создание коммерчески жизнеспособных установок искусственного прядения, использующих фосфатный триггер. По мнению Грегори Холланда, предыдущие попытки синтеза шелка терпели неудачу именно потому, что исследователи воспроизводили «ингредиенты» (белки), но не «инструкцию» (молекулярный механизм сборки). Теперь эта инструкция наконец расшифрована.
Источники
Оригинал
Читайте также
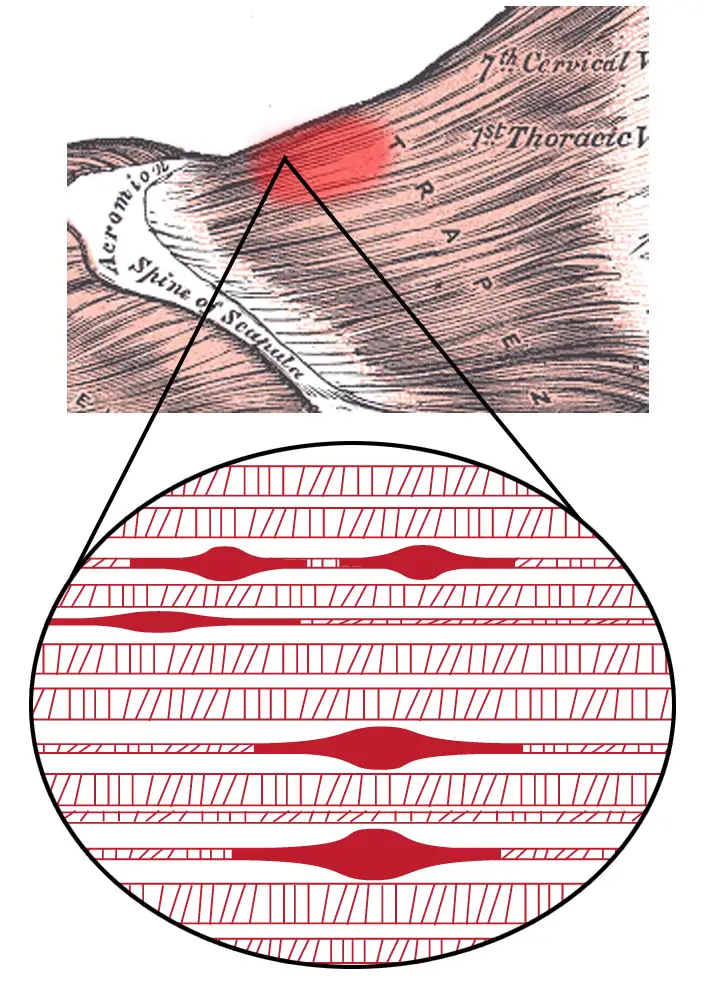
Мышечные узлы: наука о триггерных точках
Почему образуются узлы, чем опасны триггерные точки и как их лечить — молекулярный механизм COL1A1/PDGFR-α (2024).
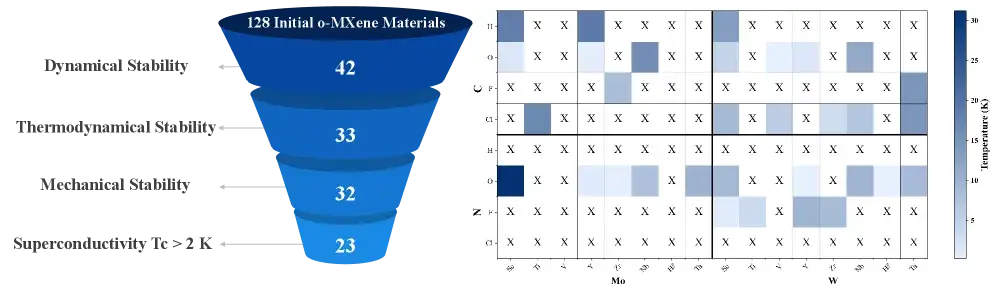
Сверхпроводник 52 K: прорыв двумерных MXенов
Учёные предсказали сверхпроводимость при 52 K в функционализированных MXенах — рекорд для двумерных материалов.
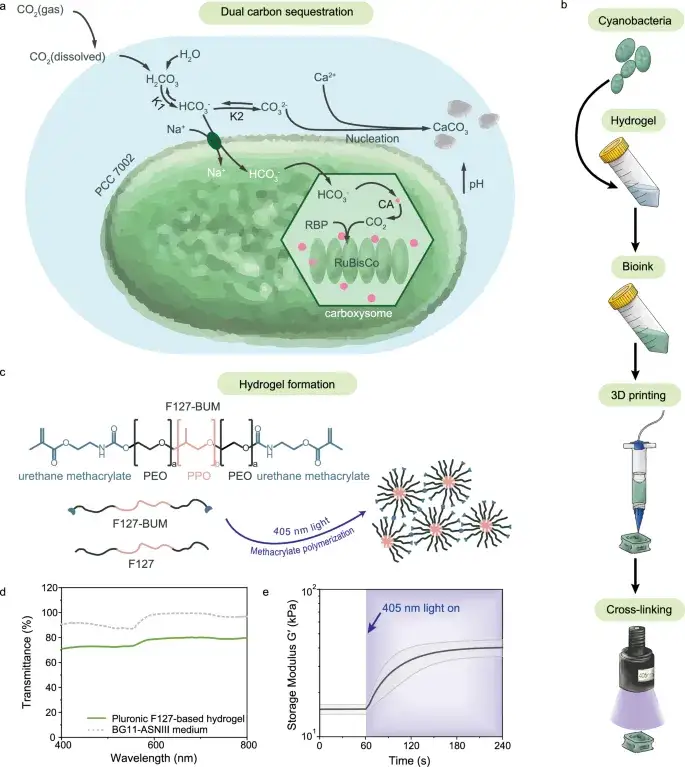
Гель с бактериями ловит CO₂ и становится прочнее (2025)
Инженеры ETH Zurich создали 3D-печатный гидрогель с цианобактериями. Он поглощает CO₂ фотосинтезом и твердеет со временем.