Недосып меняет кишечник — а кишечник разрушает мозг
Авторы: Na Zhao, Jingqi Sun, Ronghua Xu, Yafei Wang, Hao Yu, Ke An, Wenjie Zhang, Bo Jiang, Fang Xie
Представь: ты провёл три бессонные ночи подряд. Голова гудит, кофе не помогает, мир кажется чуть-чуть враждебным. Но худшее происходит не в голове — оно начинается в кишечнике. Твои кишечные бактерии уже перестроились. Баланс, который держался годами, ломается за считанные дни. И этот сломанный кишечник начинает медленно, методично повреждать твой мозг.
Звучит как сценарий фильма ужасов? Группа китайских нейробиологов под руководством Фан Сие из Третьего военно-медицинского университета в Чунцине доказала, что именно так это работает — по крайней мере у мышей. Они проследили цепочку из девяти молекулярных событий, которая начинается с нарушенного сна и заканчивается тау-патологией — тем самым признаком болезни Альцгеймера.
Пересаженные бактерии — пересаженная болезнь
Самый шокирующий момент этого исследования — не сама цепочка. А один элегантный эксперимент.
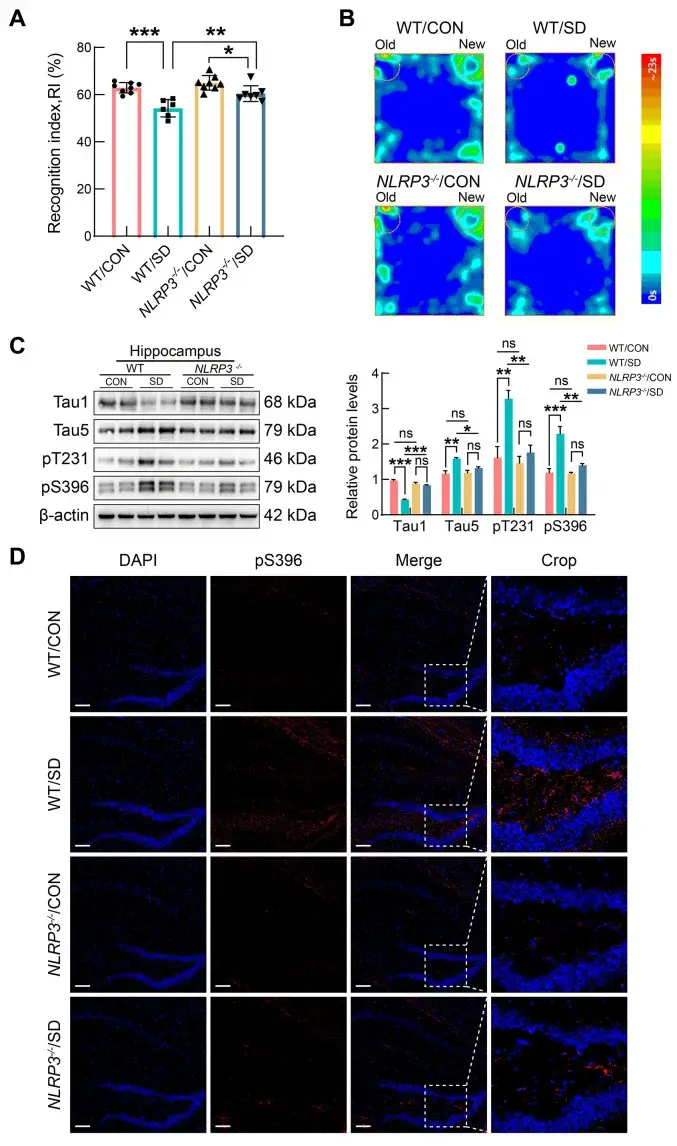
Учёные взяли кишечные бактерии у хронически недосыпающих мышей и пересадили их здоровым животным, которые спали нормально. Никакого стресса, никакого недосыпа — только чужие бактерии. Через несколько недель у здоровых мышей появились те же повреждения мозга: гиперфосфорилированный тау-белок, нейровоспаление, ослабленная аутофагия.
Аутофагия — буквально «самопоедание». Клеточный механизм уборки: клетка упаковывает повреждённые белки и органеллы в мембранные пузырьки и переваривает их. Когда аутофагия ломается, мусор накапливается — и нейроны начинают гибнуть.
Это ключевое доказательство причинно-следственной связи. Не недосып напрямую разрушает мозг — он делает это через кишечник. А значит, кишечник — не невинный свидетель, а активный участник.
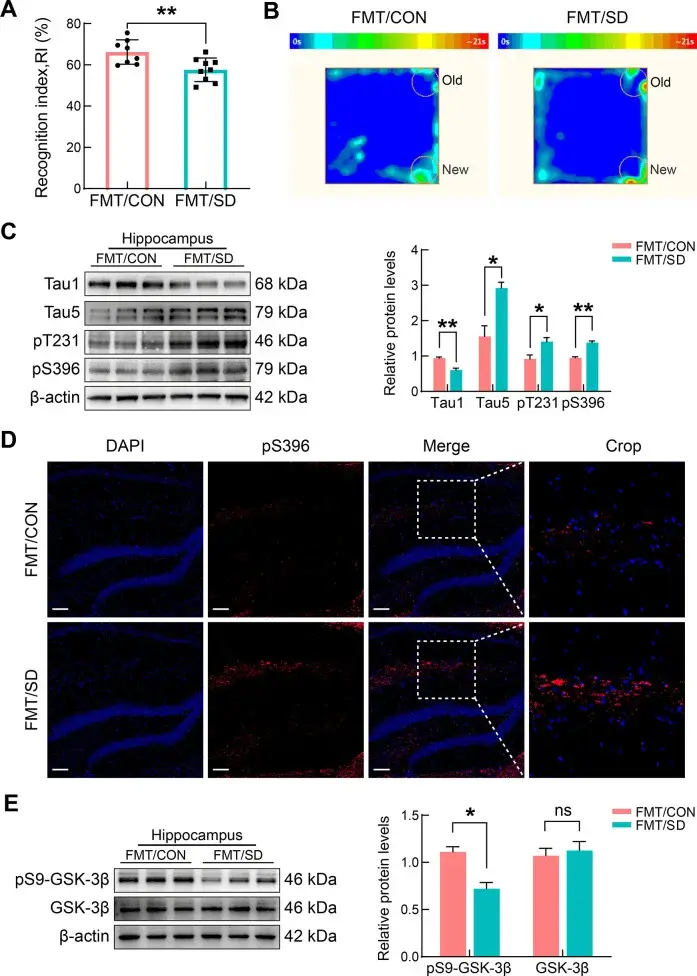
Девять домино от кишечника до мозга
Что именно происходит между первой бессонной ночью и появлением тау-клубков в нейронах? Команда Сие восстановила последовательность из девяти шагов — своего рода молекулярное домино.
Хронический недосып нарушает состав кишечной микробиоты. Защитные бактерии вроде Lactobacillus отступают, а провоспалительные виды берут верх. Повреждённая микробиота повышает проницаемость кишечного барьера — то, что в популярной литературе (не совсем корректно) называют «дырявым кишечником». Бактериальные молекулы проникают в кровоток.
Кишечный барьер — однослойная стенка клеток, выстилающая кишечник. В норме она пропускает питательные вещества и блокирует бактерии. При повреждении барьера бактериальные компоненты попадают в кровь и вызывают системное воспаление.
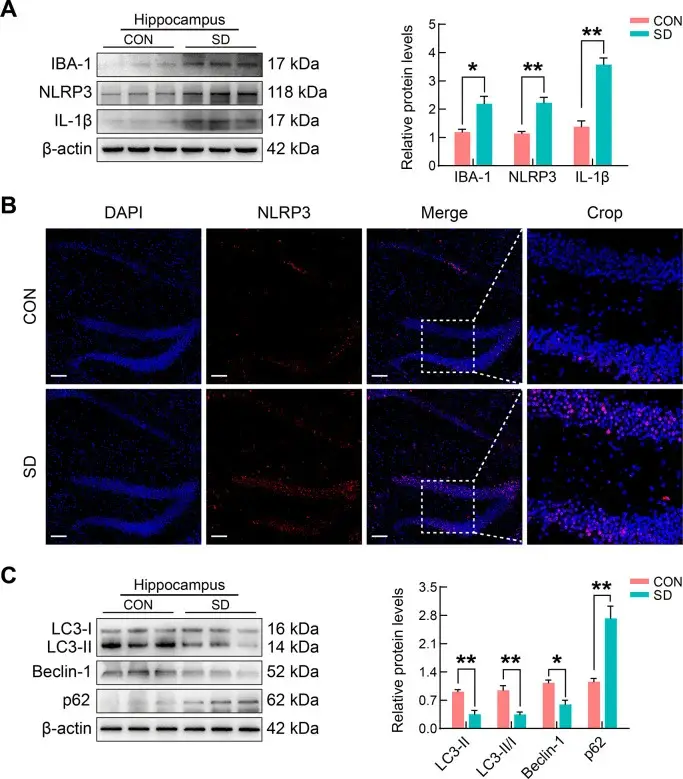
Дальше эстафету принимает иммунная система мозга. Бактериальные сигналы активируют NLRP3-инфламмасому в микроглии — резидентных иммунных клетках мозга. NLRP3 — это молекулярный детектор опасности: он собирает белковый комплекс, который запускает каскад воспаления.
Инфламмасома перехватывает управление
NLRP3-инфламмасома — мультибелковый комплекс внутри иммунных клеток. Работает как пожарная сигнализация: когда детектирует опасность (инфекцию, повреждение, токсичные белки), запускает выброс воспалительных цитокинов IL-1β и IL-18. Проблема в том, что при хроническом срабатывании «пожарная команда» сама начинает разрушать здание.
Вот здесь цепочка становится по-настоящему интересной. Активированная NLRP3-инфламмасома не просто вызывает воспаление — она подавляет аутофагию. Механизм действует через фосфорилирование белка Beclin-1, ключевого регулятора аутофагического процесса. Когда Beclin-1 заблокирован, клеточная система уборки встаёт.
Параллельно в дело вступает фермент GSK-3β. Этот белок замечателен своей двойной ролью: он одновременно активирует NLRP3-инфламмасому (усиливая воспаление) и фосфорилирует тау-белок (запуская образование нейрофибриллярных клубков). Один фермент — два удара.
Когда аутофагия отключена, а GSK-3β работает на полную мощность, гиперфосфорилированный тау-белок начинает накапливаться в нейронах. Его никто не убирает — система уборки сломана. Клубки нарастают. Нейроны начинают гибнуть.
Клеточный мусоровоз, который встал
Почему именно аутофагия оказалась слабым звеном? В здоровом мозге это мощнейшая защитная система. Она непрерывно расщепляет дефектные белки — включая агрегаты тау и бета-амилоида. Это своего рода мусоровоз, который каждый день проезжает по каждой улице.
Теперь представь, что мусоровоз встал. Мешки с мусором копятся день за днём. Через неделю улицу не пройти. Через месяц район становится непригодным для жизни. Именно это происходит с нейронами, когда Beclin-1 заблокирован: тау-белок больше не перерабатывается, а значит — накапливается, агрегирует и убивает клетку.
Команда Сие подтвердила это экспериментально. Когда мышам с повреждённой микробиотой вводили рапамицин — препарат, стимулирующий аутофагию, — тау-патология значительно уменьшалась. Мусоровоз снова выехал на маршрут.
Сколько недосыпа выдержит кишечник?
Исследование Сие использовало модель хронического недосыпа у мышей — 20 часов бодрствования в сутки на протяжении нескольких недель. Это жёсткий режим. Но что насчёт людей?
Данные по человеку пока фрагментарны, но тревожны. Кристиан Бенедикт из Уппсальского университета показал в 2016 году, что двух бессонных ночей достаточно, чтобы изменить состав кишечной микробиоты и эпигенетические метки в жировой ткани. Исследование Чжан и коллег 2017 года зафиксировало микробиомные сдвиги после пяти ночей с ограничением сна до четырёх часов.
Никто пока не прослеживал всю девятизвенную цепочку у людей — от микробиоты через NLRP3 к тау. Но каждое отдельное звено подтверждено в человеческих исследованиях: недосып меняет микробиом, повышенная проницаемость кишечника коррелирует с нейровоспалением, NLRP3 активирован при болезни Альцгеймера, нарушенная аутофагия обнаруживается в посмертных образцах мозга пациентов.
Между корреляцией и причиной
Работа опубликована в Zoological Research (июль 2024) и прошла рецензирование.
Эксперимент с трансплантацией фекальной микробиоты — сильнейший аргумент в пользу причинно-следственной связи. Он выводит исследование за рамки обычных корреляционных работ, которыми переполнена литература по оси «кишечник — мозг». Вместо «А связано с Б» мы видим «пересадка А вызывает Б».
Однако мышиный мозг — не человеческий. Мыши не болеют классической болезнью Альцгеймера: у них нет естественного накопления амилоидных бляшек и нейрофибриллярных клубков. Тау-патология в этом эксперименте — модель, а не диагноз. Переносить результаты на клинику нельзя напрямую: нам нужны проспективные когортные исследования, где сон, микробиом и когнитивный статус отслеживаются параллельно в течение лет.
Ещё одно ограничение — сама модель недосыпа. Двадцать часов бодрствования ежедневно — это экстремальный режим, редко встречающийся даже у самых отчаянных трудоголиков. Как поведёт себя цепочка при умеренном хроническом дефиците — скажем, шести часах сна вместо восьми на протяжении нескольких лет? Этот вопрос открыт.
Есть и методологический нюанс: эксперимент с трансплантацией не исключает, что вместе с бактериями пересаживаются метаболиты, фаги или другие компоненты фекального содержимого. Что именно из «посылки» запускает каскад — предстоит уточнить.
Пробиотики, сон и горизонт
Если кишечник — промежуточное звено между сном и мозгом, то теоретически на него можно воздействовать с двух сторон. Со стороны сна — очевидно: спать больше и лучше. Со стороны кишечника — через пробиотики, диету и физическую активность.
В 2025 году опубликованы результаты первого 12-недельного рандомизированного плацебо-контролируемого исследования пробиотиков у пожилых людей: мультиштаммовый препарат улучшил показатели эпизодической памяти и снизил маркеры системного воспаления. Результаты скромные, но статистически значимые. Это не лекарство от Альцгеймера — но, возможно, один из кирпичиков профилактики.
Физическая активность действует на ту же ось с другой стороны: метаанализ 2023 года показал, что регулярные аэробные упражнения увеличивают разнообразие кишечной микробиоты и снижают маркеры нейровоспаления. Механизм, вероятно, пересекается с тем, что описали Сие и коллеги: здоровый микробиом — менее активная NLRP3 — работающая аутофагия — меньше тау-агрегатов.
Главный вопрос на горизонте — можно ли поймать цепочку в начале и разорвать её, пока повреждения обратимы? Ответ определит, станет ли ось «сон — кишечник — мозг» мишенью для реальной терапии или останется красивой схемой в учебниках нейробиологии.
Часто задаваемые вопросы
Действительно ли плохой сон может привести к болезни Альцгеймера?
Прямая причинно-следственная связь у людей пока не доказана. Однако эпидемиологические данные последовательно показывают, что хронический дефицит сна ассоциирован с повышенным риском деменции. Исследование Сие впервые описало полную молекулярную цепочку — от недосыпа через кишечник к тау-патологии — но пока только на мышах.
Помогут ли пробиотики защитить мозг от последствий недосыпа?
Первые клинические данные обнадёживают: 12-недельный курс пробиотиков улучшил память у пожилых людей в рандомизированном исследовании 2025 года. Но конкретно для защиты мозга от недосыпа пробиотики не тестировались. Это перспективное направление, но рекомендовать конкретные штаммы преждевременно.
Через какое время недосып начинает влиять на кишечник?
У людей изменения в составе кишечной микробиоты фиксируются уже после двух ночей без сна. При пяти ночах с ограничением до четырёх часов сна сдвиги ещё заметнее. Однако насколько быстро эти изменения становятся клинически значимыми — неизвестно.
Что такое ось «кишечник — мозг» и почему она важна?
Это двусторонний канал связи между кишечной микробиотой и центральной нервной системой. Он работает через блуждающий нерв, иммунные сигналы и метаболиты бактерий. Нарушение баланса кишечных бактерий может влиять на воспаление в мозге, настроение и когнитивные функции. Исследование Сие показало, что этот канал может передавать и нейродегенеративные сигналы.
Можно ли «починить» повреждения мозга, если начать высыпаться?
В эксперименте на мышах стимуляция аутофагии рапамицином уменьшала тау-патологию, что намекает на обратимость. Но у людей нет данных о том, восстанавливается ли повреждение после нормализации сна. Вероятно, на ранних стадиях система способна к восстановлению, но при длительном хроническом недосыпе часть повреждений может стать необратимой.
Источники
Связанные
- Acute sleep loss results in tissue-specific alterations in genome-wide DNA methylation state and metabolic fuel utilization in man (Science Advances)
- Sleep Deprivation and Gut Microbiota Dysbiosis: Current Understandings and Implications (Int. J. Mol. Sci.)
- Effects of a probiotic supplement on cognitive function in healthy older adults: a 12-week RCT (Nutrients, 2025)
Читайте также
Кофе против деменции: Гарвард проверил 132 000 человек за 40 лет
Крупнейшее наблюдательное исследование в JAMA: 2–3 чашки кофе или 1–2 чашки чая в день связаны с 18% снижением риска деменции. Декаф не помогает — и это говорит о чём-то важном.
Бактерии против рака: клостридии научили пожирать опухоли
Инженеры научили Clostridium sporogenes находить опухоль, собираться в колонию и уничтожать рак изнутри — живое оружие против неоперабельных опухолей.
Бактерия из 5000-летнего льда устойчива к 10 антибиотикам — и может подсказать новые
В румынской пещере нашли микроб возрастом 5000 лет, устойчивый к 10 антибиотикам. Его гены — ключ к созданию новых лекарств.