Мышечные узлы: наука о триггерных точках
Авторы: Yu Liu, Feng Qi
Зачем это важно
Каждый, кто хоть раз щупал свою шею после долгого рабочего дня, знает это ощущение: жёсткий, болезненный комок где-то между лопаткой и позвоночником. Надавишь — и боль отдаёт куда-то в висок, руку или вниз по спине. Это и есть то, что в обиходе называют «мышечный узел», а в медицине — миофасциальная триггерная точка.
По разным оценкам, миофасциальным болевым синдромом страдает до 30% населения планеты. Это одна из самых частых причин хронической боли в шее, спине и плечах — но, как ни странно, учёные до сих пор спорят, что именно представляют собой эти «узлы» и почему они появляются.
В 2024 году команда из Университета Шаньдун опубликовала в журнале Anesthesiology работу, которая впервые описала конкретный молекулярный механизм образования мышечных узлов. Открытие оси COL1A1/PDGFR-α/JAK2/STAT3 — это не просто очередная гипотеза, а экспериментально подтверждённый путь от молекулы до боли. И потенциально — ключ к принципиально новым методам лечения.
Классическая теория: энергетический кризис
Чтобы понять прорыв 2024 года, нужно сначала разобраться в том, что мы «знали» раньше.
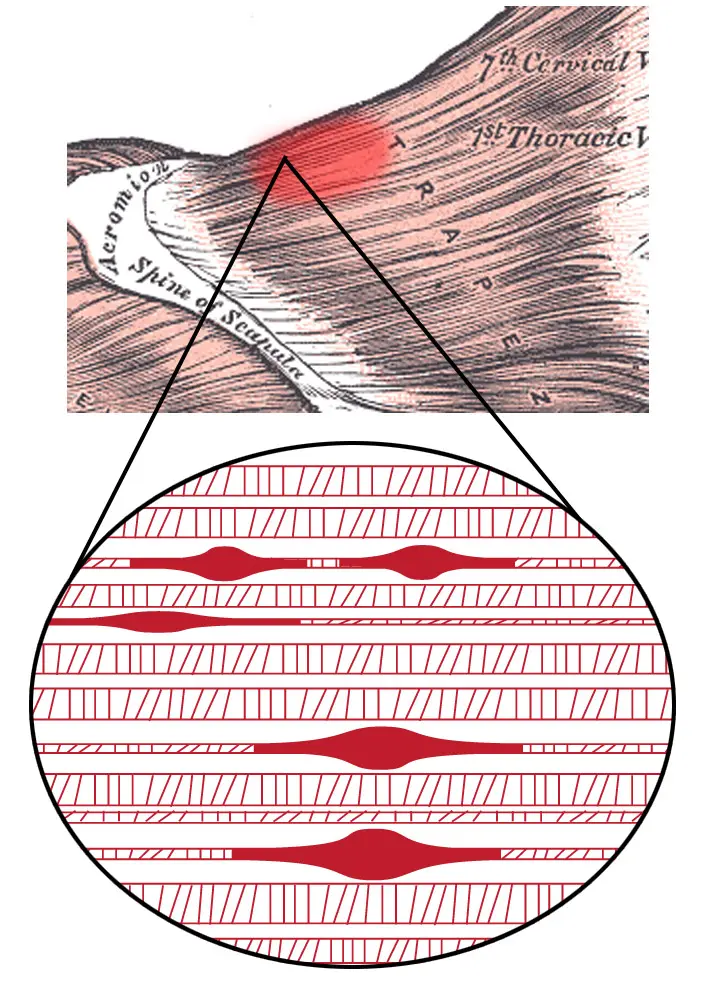
Миофасциальная триггерная точка (МТрТ) — гиперраздражимый узелок в пределах тугой полоски скелетной мышцы. При надавливании вызывает локальную боль, отражённую боль в отдалённые зоны, а иногда — непроизвольное подёргивание мышечного пучка.
Классическая «интегрированная гипотеза» Дэвида Саймонса, сформулированная ещё в 1990-х, описывает мышечный узел как порочный круг:
- Пусковое событие — микротравма, перегрузка, длительное статическое напряжение
- Избыток ацетилхолина — нервно-мышечная концевая пластинка начинает выбрасывать слишком много нейромедиатора
- Застрявшее сокращение — несколько саркомеров намертво застревают в укороченном состоянии
- Ишемия — спазмированный участок пережимает капилляры, кровоток падает
- Энергетический кризис — без кислорода падает синтез АТФ, а без АТФ кальциевый насос не может расслабить мышечное волокно
- Боль — гипоксия и повреждение тканей высвобождают «коктейль» из медиаторов боли: субстанция P, брадикинин, простагландины, цитокины
Саркомер — минимальная сократительная единица мышцы. Представьте два набора гребней, вставленных друг в друга. Когда мышца сокращается, эти «гребни» — белки актин и миозин — скользят друг по другу, укорачивая саркомер. Чтобы разойтись обратно, нужна энергия в виде АТФ.
Модель красивая и логичная. Но вот проблема: она описывает замкнутый круг, не объясняя, что именно на молекулярном уровне запускает и поддерживает это состояние. Электрофизиологи десятилетиями фиксировали спонтанную электрическую активность в зонах триггерных точек — но что стоит за ней?
Прорыв: ось COL1A1 → PDGFR-α → JAK2/STAT3
В июле 2024 года Юй Лю и коллеги из Университета Шаньдун задали простой, но до них почему-то не исследованный вопрос: если триггерная точка — это патологический процесс в ткани, то какие рецепторные тирозинкиназы в ней активированы?
Рецепторные тирозинкиназы (RTK) — белки-рецепторы на поверхности клеток, которые при активации запускают каскады внутриклеточных сигналов. Это своего рода «антенны», принимающие молекулярные сообщения. PDGFR-α — один из таких рецепторов, обычно связанный с ростом клеток и заживлением ран.
Исследователи взяли биопсию верхней трапециевидной мышцы у 11 пациентов с хронической миофасциальной болью и 7 здоровых добровольцев. С помощью микрочипа фосфорилирования RTK они проверили активность десятков рецепторов одновременно — и обнаружили, что один из них резко выделяется на фоне остальных.
PDGFR-α — рецептор тромбоцитарного фактора роста альфа. Его активация в тканях триггерных точек была достоверно повышена (p < 0.001). Более того, уровень активированного PDGFR-α коррелировал с интенсивностью боли по визуально-аналоговой шкале (r = 0.711). Чем сильнее болит — тем больше фосфорилированного рецептора в ткани.
Но кто активирует этот рецептор? Классический лиганд PDGFR-α — это белок PDGF-AA. Его уровень в крови у пациентов тоже был повышен (5.97 нг/мл против 3.74 у контроля). Однако настоящий сюрприз ждал дальше.
Коллаген как сигнальная молекула
Используя масс-спектрометрию и ко-иммунопреципитацию, авторы обнаружили, что PDGFR-α физически связывается с COL1A1 — коллагеном I типа, основным структурным белком соединительной ткани.
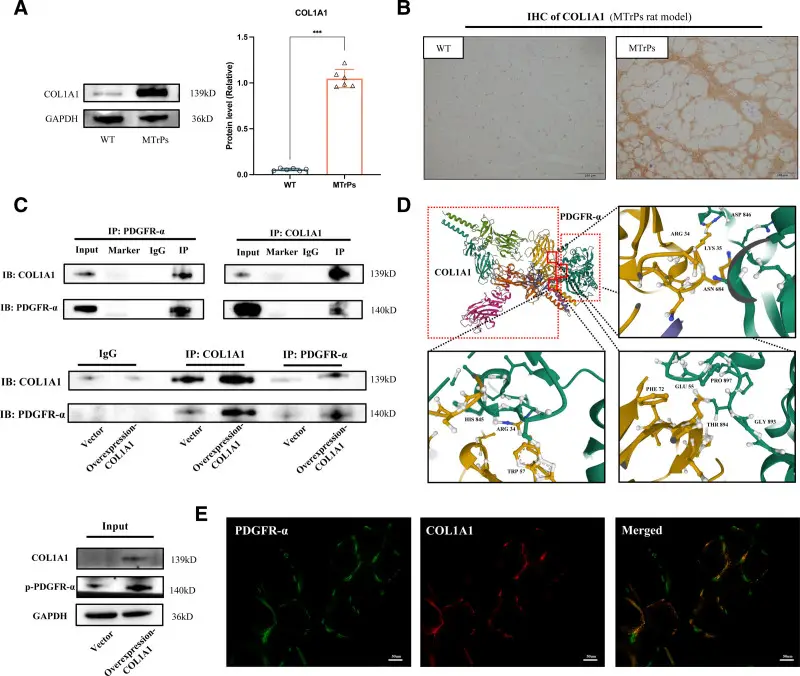
Это было неожиданно. Коллаген I — это «каркасный» белок, который все привыкли воспринимать как пассивную конструкцию, своего рода арматуру тканей. Но оказалось, что COL1A1 работает ещё и как сигнальная молекула: он связывается с PDGFR-α и активирует его напрямую, без классического лиганда PDGF.
Молекулярный докинг показал конкретные точки связывания: аминокислоты LYS35–ASP846, GLU55–THR894, HIS845–ARG34.
От молекулы к боли
Дальше авторы проверили всю цепочку на крысиной модели. Каскад начинается с накопления COL1A1 в зоне повреждённой мышцы — при микротравмах, перегрузке или хроническом напряжении. Избыток коллагена связывается напрямую с PDGFR-α, запуская его фосфорилирование, а тот, в свою очередь, активирует сигнальный путь JAK2/STAT3 — классический каскад воспаления. Дальше происходят два параллельных процесса: провоспалительные цитокины (IL-1β, IL-6, TNF-α) заливают локальную ткань, а киназа лёгких цепей миозина (MLCK) фосфорилирует миозин, запирая саркомеры в устойчивом сокращении. Волокна укорачиваются с нормальных 2.13 мкм до 1.63 мкм. Конечный результат — contraction knot, узел сокращения: самоподдерживающийся цикл спазма, воспаления и боли.
JAK2/STAT3 — один из ключевых внутриклеточных сигнальных путей. JAK2 — фермент-киназа, который при активации фосфорилирует транскрипционный фактор STAT3. Активированный STAT3 проникает в ядро клетки и включает гены воспаления и сокращения. Этот путь хорошо известен в онкологии — и теперь оказалось, что он причастен к мышечной боли.
Самое важное: когда исследователи заблокировали этот путь — либо нокдауном PDGFR-α, либо ингибитором JAK2/STAT3 (препарат AZD1480) — болевое поведение у крыс уменьшалось, саркомеры восстанавливали нормальную длину, а уровень воспалительных цитокинов падал.
Чем опасны мышечные узлы
«Подумаешь, напряжение в шее» — скажет кто-то. Но миофасциальные триггерные точки — это не просто дискомфорт, а пусковой механизм целой цепочки последствий, которые уходят далеко за пределы больного места.
Самое коварное — хронизация боли. Непрерывный поток сигналов из триггерных точек перестраивает спинной мозг через центральную сенситизацию: нервная система постепенно «выкручивает громкость», пока стимулы, которые раньше не замечались, не начинают причинять боль. Врачи называют это аллодинией — и она означает, что порог боли продолжает снижаться задолго после того, как исходная травма зажила.
Хуже того, одна триггерная точка редко остаётся одинокой. Она стремится активировать сателлитные точки в соседних мышцах, мышцах-антагонистах и порой совсем далёких областях. Пациент, который пришёл с болью в шее, через полгода обнаруживает болезненные уплотнения в пояснице и бёдрах — не новая травма, а старая проблема, распространяющаяся по мышечным цепям.
А дальше включаются вторичные эффекты: хроническая боль разрушает архитектуру сна, плохой сон усиливает чувствительность к боли, и оба фактора повышают риск тревоги и депрессии — которые, в свою очередь, увеличивают мышечное напряжение. Три замкнутых круга, вложенных друг в друга. Тем временем поражённые мышцы теряют подвижность, вынуждают тело принимать щадящие позы и слабеют. Исследования трапециевидной мышцы показывают, что триггерные точки достоверно ограничивают подвижность шеи и повышают частоту хронических головных болей напряжения.
Научный спор: существуют ли триггерные точки?
Тема триггерных точек — одна из самых спорных в медицине, и накал дискуссии может удивить.
Скептики во главе с Джоном Квинтнером из IASP (Международная ассоциация по изучению боли) указывают на серьёзные проблемы:
- Разные специалисты, пальпируя одного и того же пациента, часто находят триггерные точки в разных местах
- Эффекты лечения сложно отличить от плацебо
- Диагностика строится на круговой логике: «болит → нашли болезненную точку → значит, точка вызывает боль»
Сторонники парируют:
- Биохимические изменения в зонах триггерных точек воспроизводимы — субстанция P, цитокины, локальный ацидоз
- УЗИ-эластография 2024 года показала, что триггерные точки объективно жёстче окружающей ткани и имеют измеримые параметры
- Свежая работа Liu et al. впервые даёт конкретный молекулярный механизм
Современный компромисс (к 2024–2025): болезненные мышечные уплотнения — реальный клинический феномен. Но это, вероятно, не отдельная «болезнь», а комбинация локальных мышечных изменений и общей чувствительности нервной системы. Работа про PDGFR-α подкрепляет «периферическую» составляющую — но роль центральной сенситизации в хронизации остаётся ключевой.
Как избавиться: что говорит наука
Систематические обзоры 2024–2025 годов позволяют составить иерархию методов по силе доказательств:
Сухое иглоукалывание (dry needling) — наиболее изученный метод. Мета-анализы показывают умеренно-выраженное краткосрочное уменьшение боли и повышение болевого порога. Эффект сохраняется до 6 недель. Требует обученного специалиста.
Dry needling — введение тонкой иглы непосредственно в триггерную точку. В отличие от акупунктуры, здесь нет «меридианов» — игла целенаправленно попадает в зону спазма, вызывая локальное подёргивание и последующее расслабление мышечного пучка.
Массаж и мануальная терапия — умеренные доказательства. Фрикционный массаж триггерных точек повышает болевой порог и увеличивает объём движений. Несколько сеансов работают лучше, чем один. Безопасно, доступно, хорошо сочетается с упражнениями.
Ударно-волновая терапия (ESWT) — появляются данные об эффективности при триггерных точках в пояснице. Качество доказательств пока низкое–умеренное.
Foam rolling и самомассаж — уменьшает болезненность и улучшает подвижность в краткосрочной перспективе. Но строгих данных именно по клиническим триггерным точкам мало. Дёшево, безопасно и удобно для ежедневного использования.
Упражнения — ключевой компонент любого протокола. Растяжка + укрепление целевых мышц + коррекция эргономики. Без этого все остальные методы дают только временный эффект.
Инъекции в триггерные точки — мета-анализ 2023 года показал умеренное преимущество перед медикаментозной терапией при острой миофасциальной боли. Используют лидокаин, ботулотоксин, или просто физраствор — интересно, что эффект «сухой иглы» часто сравним с инъекцией.
Критический взгляд
Главное методологическое достоинство работы в том, что авторы не начинали с заранее выбранной гипотезы. Вместо того чтобы проверять, например, роль субстанции P или брадикинина, команда запустила непредвзятый RTK-скрининг сразу по десяткам рецепторов одновременно — и дала данным самим указать на PDGFR-α. Такой агностический дизайн делает результат значительно более устойчивым к обвинениям в предвзятости подтверждения. Не менее важна причинно-следственная архитектура доказательной базы: авторы не остановились на корреляции. Они заблокировали PDGFR-α генетически и подавили JAK2/STAT3 фармакологически препаратом AZD1480 — в обоих случаях болевое поведение снижалось, длина саркомеров нормализовалась, а уровень воспалительных цитокинов падал. Биопсийный подход — сравнение активной триггерной ткани со здоровой мышцей из той же анатомической области — также устраняет многие межгрупповые факторы смешения, которые так осложняют исследования боли.
Однако человеческие данные стоят на шатком фундаменте: 11 пациентов и 7 контролей из одной университетской клиники. Выборка такого размера может зафиксировать сигнал, но не способна ответить на вопрос, является ли ось COL1A1/PDGFR-α универсальным механизмом всех миофасциальных триггерных точек или лишь одним из нескольких путей, актуальных только для определённого подтипа пациентов или характера травмы. Животная модель несёт собственные ограничения: тупая травма икроножной мышцы крысы удобна для получения узлов сокращения, но лишь приблизительно воспроизводит хроническую низконагрузочную перегрузку, которая порождает большинство человеческих триггерных точек. История трансляции крысиных болевых исследований в клиническую практику крайне неоднородна — поведенческая релевантность пути у людей пока не подтверждена независимыми когортами.
Наиболее принципиальный открытый вопрос носит механистический, а не клинический характер: как этот новый молекулярный каскад взаимодействует с уже работающими методами лечения? Сухое иглоукалывание, массаж и упражнения доказанно снижают боль при триггерных точках, но ни один из них не разрабатывался с прицелом на PDGFR-α. Понять, подавляют ли эти вмешательства накопление COL1A1, прерывают ли JAK2/STAT3-сигнализацию или действуют через совершенно иные механизмы, — значит разом продвинуть и науку, и терапию. Что касается прямого применения ингибиторов PDGFR-α или JAK2/STAT3: препараты класса JAK-ингибиторов (руксолитиниб, барицитиниб) уже одобрены в ревматологии и онкологии, что сокращает доклинический путь, — но локальное введение при мышечной боли всё равно потребует многолетних испытаний на безопасность и подбор дозировок.
Исследование опубликовано в рецензируемом журнале Anesthesiology (IF ~9), однако для окончательных выводов нужна независимая репликация. Эта статья — научно-популярный обзор, а не медицинская рекомендация.
Что дальше
Открытие оси COL1A1/PDGFR-α/JAK2/STAT3 открывает несколько направлений:
Новые терапевтические мишени. Ингибиторы JAK2 уже существуют — руксолитиниб, барицитиниб, тофацитиниб. Они применяются в ревматологии и онкологии. Теоретически, локальное введение таких препаратов в зону триггерной точки может быть эффективнее существующих инъекций. Но это пока чистая гипотеза.
Объективная диагностика. Если уровень фосфорилированного PDGFR-α коррелирует с интенсивностью боли, это может стать первым объективным биомаркером миофасциальной боли — вместо субъективной пальпации.
Мост между лагерями. Данные Liu et al. могут примирить скептиков и сторонников триггерных точек: есть объективный молекулярный субстрат, но он тесно связан с нейровоспалением и центральной сенситизацией. Обе стороны спора отчасти правы.
А пока, если у вас сейчас болит шея — встаньте, потянитесь, подвигайте плечами. Упражнения — единственный метод с нулевой стоимостью и нулевыми побочными эффектами, который работает и при «загадочных триггерных точках», и при «просто напряжённых мышцах». Какой бы из лагерей ни оказался прав.
Часто задаваемые вопросы
Мышечные узлы — это то же самое, что мышечный спазм?
Нет. Мышечный спазм — это непроизвольное сокращение всей мышцы или её большого участка, обычно кратковременное. Мышечный узел — это устойчивое сокращение нескольких саркомеров в пределах одного мышечного пучка. Он может сохраняться неделями и месяцами, в отличие от спазма, который обычно проходит за минуты.
Можно ли самостоятельно определить триггерную точку?
Типичные признаки при самопальпации: плотный узелок в мышце, резкая болезненность при надавливании, боль отдаёт в другую область — например, из шеи в висок. Однако исследования показывают, что даже профессионалы не всегда согласны друг с другом при пальпации. Если боль хроническая или сильно влияет на качество жизни — стоит обратиться к специалисту, а не полагаться на самодиагностику.
Правда ли, что стресс вызывает мышечные узлы?
Да, связь подтверждена исследованиями. Психологический стресс повышает тонус мышц через активацию симпатической нервной системы, ухудшает микроциркуляцию и снижает болевой порог. У студентов в период экзаменов, например, достоверно чаще обнаруживаются активные триггерные точки в трапециевидной мышце. Но стресс — скорее поддерживающий фактор, а не единственная причина.
Насколько эффективен foam roller против триггерных точек?
Foam rolling умеренно уменьшает мышечную болезненность и улучшает подвижность — это подтверждают систематические обзоры. Однако строгих данных именно по клиническим триггерным точкам мало. Foam roller — хороший инструмент ежедневной профилактики, но при стойкой хронической боли он вряд ли заменит целенаправленный массаж, dry needling или программу упражнений.
Когда ожидать новых лекарств на основе открытия PDGFR-α?
Не скоро. Результаты Liu et al. — это базовая наука: доказан молекулярный механизм на крысах и небольшой группе пациентов. До клинических испытаний целенаправленной терапии нужны годы дополнительных исследований — проверка на большей выборке, оценка безопасности локального введения ингибиторов JAK2, разработка протоколов дозирования. Оптимистичная оценка — 5–10 лет до появления первых клинических протоколов.
Источники
Связанные
- Advancing musculoskeletal diagnosis and therapy: a comprehensive review of trigger point theory and muscle pain patterns
- Myofascial Pain Syndrome: An Update on Clinical Characteristics, Etiopathogenesis, Diagnosis, and Treatment
- Myofascial trigger points: spontaneous electrical activity and its consequences for pain induction and propagation
- Mechanisms of Myofascial Pain
- Myofascial trigger point (MTrP) size and elasticity properties can be used to differentiate characteristics of MTrPs in lower back skeletal muscle
- Treating myofascial pain with dry needling: a systematic review
- The effect of friction massage on pain intensity, PPT, and ROM in individuals with myofascial trigger points
Читайте также
Бактерии пожирают рак: прорыв клостридий
Клостридии научили находить опухоль, собираться в колонию и уничтожать рак изнутри — оружие против неоперабельных опухолей.
Большая пятёрка личности: 254 гена и шестой фактор (2025)
Геномное исследование 600 000 человек нашло 254 гена личности. Шестой фактор за пределами Big Five предсказывает смертность.
Паучий шёлк прочнее стали в 5 раз: секрет раскрыт
Учёные расшифровали точный молекулярный переключатель — связи аргинин-тирозин — превращающий жидкий белок в нить прочнее стали.