Бактерии против рака: клостридии научили пожирать опухоли
Авторы: Sara Sadr, Bahram Zargar, Marc G. Aucoin, Brian Ingalls
В 1891 году нью-йоркский хирург Уильям Коли сделал нечто, что ужаснуло медицинское сообщество: он взял живые стрептококки и ввёл их прямо в неоперабельную опухоль пациента. Коллеги решили, что он сошёл с ума. Но у нескольких больных опухоли начали уменьшаться.
135 лет спустя инженеры из канадского Университета Уотерлу наконец превратили эту «безумную» идею в управляемую технологию. Они взяли почвенную бактерию Clostridium sporogenes, научили её выживать в присутствии кислорода и — главное — дали ей нечто вроде социальной сети: систему кворум-сенсинга, благодаря которой бактерии «голосуют» за то, когда начать атаку.
Самый безумный эксперимент в истории онкологии
Уильям Коли не знал, почему его метод иногда работает. Он просто заметил закономерность: у пациентов, перенёсших тяжёлую бактериальную инфекцию рядом с опухолью, рак иногда отступал. Коли начал целенаправленно заражать больных смесью бактерий — «токсинами Коли» — и за 40 лет своей практики задокументировал десятки случаев ремиссии.
Токсины Коли (Coley’s toxins) Смесь убитых бактерий Streptococcus pyogenes и Serratia marcescens, которую Уильям Коли вводил онкологическим пациентам с 1891 по 1936 год. Считается первой формой иммунотерапии рака — задолго до появления самого термина.
Его метод был грубым, непредсказуемым и часто опасным. С появлением лучевой терапии и химиотерапии в середине XX века «токсины Коли» были забыты. Но идея о том, что бактерии способны уничтожать опухоли, не умерла — она ушла в подполье.
Незваные гости в опухолях
В 1950-х годах исследователи обнаружили нечто удивительное: споры бактерий рода Clostridium при внутривенном введении попадали в организм, но прорастали исключительно в одном месте — внутри солидных опухолей.
Причина оказалась в физике самих опухолей. Когда злокачественная опухоль растёт быстрее, чем к ней подрастают сосуды, в её центре образуется зона без кровоснабжения — некротическое ядро. Там нет кислорода, нет иммунных клеток, почти нет питательных веществ. Для большинства организмов это мёртвая зона. Но не для клостридий.
Некротическое ядро (necrotic core) Бескислородная зона в центре крупных солидных опухолей, где клетки погибли из-за недостатка кровоснабжения. Недоступна для большинства лекарств и иммунных клеток — именно поэтому многие опухоли рецидивируют после лечения.
Clostridium — строгие анаэробы. Они не просто выживают без кислорода — они в нём нуждаются. Точнее, наоборот: кислород для них токсичен. Некротическое ядро опухоли — для них идеальный дом.
Это давало невероятно точный «адрес доставки»: бактерии сами находили опухоль и селились именно там, куда не добираются ни химиотерапия, ни иммунные клетки. Звучит как идеальное оружие. Но была проблема — и не одна.
Клинические попытки: успех с привкусом сепсиса
В 1990-х родилась концепция CDEPT — Clostridium-directed enzyme prodrug therapy. Идея элегантная: бактерии доставляют в опухоль фермент, который превращает безвредное пролекарство в токсин прямо на месте. Химиотерапия точечного действия, активируемая живым «курьером».
CDEPT (Clostridium-directed enzyme prodrug therapy) Метод, при котором генетически модифицированные клостридии доставляют фермент в опухоль. Затем пациент получает безвредное пролекарство, которое этот фермент превращает в цитотоксин — но только внутри опухоли.
В 2010-х команда из Университета Джонса Хопкинса под руководством Шибина Чжоу вывела клинические испытания на новый уровень. Они использовали C. novyi-NT — штамм, из которого удалили главный токсин. В Фазе I/Ib клинических испытаний (NCT01924689) споры вводили напрямую в опухоли 24 пациентов.
Результаты были впечатляющими — и пугающими одновременно. У 42–46% пациентов споры успешно проросли в опухолях. У 86% наблюдалась стабилизация заболевания. Но некоторые пациенты получили тяжёлые осложнения: газовую гангрену, сепсис, абсцессы.
Фундаментальная проблема была в том, что бактерии оставались «тупыми». Они не могли определить, когда их достаточно для атаки. Не могли перестать расти, когда опухоль уже разрушена. Не могли адаптироваться к смешанной среде — где-то в опухоли кислород есть, где-то нет. Это были мощные, но неуправляемые биологические снаряды.
Два ключа от Уотерлу
Команда из Университета Уотерлу под руководством Бахрама Заргара и Брайана Инглза пошла другим путём. Вместо C. novyi-NT они выбрали C. sporogenes — родственный вид, с которым проще работать в лаборатории. И поставили амбициозную цель: сделать бактерию не только эффективной, но и умной.
Первый ключ появился в 2023 году. Аспирантка Сара Садр и её коллеги встроили в C. sporogenes ген, заимствованный у родственного микроорганизма, который позволял бактерии кратковременно выживать в присутствии кислорода. Это решало критическую проблему: при внутривенном введении споры неизбежно проходят через насыщенные кислородом ткани. Без защиты они гибли бы на подступах к опухоли.
Второй ключ — и это прорыв, опубликованный в декабре 2025 года в журнале ACS Synthetic Biology — оказался ещё изящнее.
Бактериальная демократия
Представьте, что вы — бактерия. Вы попали в организм, нашли некротическое ядро опухоли и начали размножаться. Но откуда вам знать, что вас уже достаточно для атаки? Что пора включать «боевой режим»?
Вот здесь в дело вступает кворум-сенсинг — одна из самых элегантных систем коммуникации в живой природе.
Кворум-сенсинг (quorum sensing) Механизм «бактериальной демократии»: клетки непрерывно выделяют сигнальные молекулы. Когда концентрация этих молекул достигает порога (то есть рядом достаточно «избирателей»), запускается коллективное изменение поведения — например, активация генов вирулентности или биолюминесценция.
Садр и коллеги взяли систему кворум-сенсинга agr из Staphylococcus aureus — хорошо изученную и надёжную — и пересадили её в C. sporogenes. Это всё равно что дать бактериям мобильный телефон и групповой чат.
Каждая бактерия непрерывно выделяет небольшой сигнальный пептид (AIP — autoinducing peptide). Пока бактерий мало, концентрация AIP низкая — и ничего не происходит. Бактерии живут, размножаются, но молчат. Но когда популяция достигает критической массы, концентрация сигнала пересекает порог — и у всех бактерий одновременно включаются целевые гены.
В данном исследовании вместо терапевтического гена учёные использовали GFP — зелёный флуоресцентный белок. Это индикатор: если бактерии начали светиться зелёным, значит, кворум-сенсинг работает. И он заработал. При достижении пороговой плотности популяции C. sporogenes дружно включали GFP — подтверждая, что гетерологичная система agr функционирует в новом хозяине.
Живое программируемое оружие
Зачем всё это? Потому что кворум-сенсинг — это не просто научная игрушка. Это встроенный предохранитель.
Вспомните главную проблему клинических испытаний C. novyi-NT: бактерии неконтролируемо росли и вызывали сепсис. Теперь представьте систему, в которой терапевтический ген (например, фермент для CDEPT или цитокин, разрушающий опухоль) активируется только при достаточной плотности бактерий — то есть только внутри опухоли.
Если одна бактерия случайно попадёт в здоровую ткань — ничего не произойдёт. Она одна, кворума нет, опасные гены молчат. Это принципиально другой уровень безопасности.
А в сочетании с кислородной устойчивостью получается платформа:
- Споры вводят внутривенно — ген кислородной толерантности позволяет пережить транспорт через кровь
- Споры находят опухоль — прорастают только в бескислородном некротическом ядре
- Бактерии размножаются — и «голосуют» через кворум-сенсинг
- Кворум достигнут — активируется терапевтический ген
- Опухоль разрушается изнутри
Причём терапевтическую «боеголовку» можно менять: ферменты для пролекарств, цитокины для активации иммунитета, токсины для прямого уничтожения клеток. Модульная платформа — как конструктор.
Критический взгляд
Исследование Садр и коллег — proof of concept, а не готовое лекарство. Дистанция между этими двумя понятиями — огромная.
Подлинная значимость работы определяется её местом в истории поля. Успешная трансплантация системы кворум-сенсинга agr в C. sporogenes — это видовая новизна: до этого никто подобного не делал. Выбор именно agr не случаен: десятилетия исследований S. aureus создали на редкость полную картину того, как работает этот генетический контур, что снижает риск непредсказуемого поведения в новом хозяине. Не менее важен модульный принцип: использование GFP в роли репортёра вместо терапевтического гена — сознательный акт научной сдержанности, который делает систему простой в верификации и лёгкой в модификации. Две взаимосвязанные публикации — 2023 и 2025 года, каждая из которых надстраивает предыдущую, — свидетельствуют о дисциплинированной долгосрочной стратегии, а не об одноразовой публикации ради публикации.
Ограничения, однако, — это не мелкие оговорки: они задают реальную дистанцию до пациента. Модификация кислородной устойчивости и схема кворум-сенсинга существуют в разных штаммах и пока не объединены в одном организме. Все эксперименты проведены in vitro — данных на животных не существует вообще; реакция иммунной системы на инженерные клостридии, колонизирующие опухоль, полностью неизвестна. Эволюционная стабильность — отдельная проблема: бактерии быстро размножаются и способны избавляться от чужеродного генетического материала. Сохранятся ли встроенные контуры под давлением отбора внутри живого организма — вопрос, который текущая работа не может даже поставить, не то что решить.
За лабораторным горизонтом скрываются и более глубокие неопределённости. Что произойдёт с бактериями после разрушения опухоли, когда кислород зальёт бывшее некротическое ядро — погибнут ли они сами, или потребуется синтетический «kill switch»? Каков минимальный размер опухоли, необходимый для формирования достаточно большого некротического ядра? И, пожалуй, самый тревожный с точки зрения биобезопасности вопрос: способен ли горизонтальный перенос генов распространить инженерные возможности на другие микроорганизмы — в кишечнике или в окружающей среде? Это не гипотетические препятствия — это реальные этапы, стоящие между нынешним результатом и клиническими испытаниями.
Данный анализ основан на публикации в рецензируемом журнале ACS Synthetic Biology (IF ~5.0). Статья прошла peer review, но описывает ранний этап разработки — in vitro эксперименты. До клинического применения необходимы годы дополнительных исследований.
Что дальше
Ближайший шаг команды из Уотерлу — объединить оба модификации в одном штамме C. sporogenes и заменить GFP-репортёр на терапевтический ген. Затем — доклинические испытания на мышиных моделях солидных опухолей.
Параллельно в мире идёт несколько клинических испытаний бактериальной терапии рака. C. novyi-NT от компании BioMed Valley Discoveries (Фаза II, NCT03435952) остаётся наиболее продвинутым кандидатом. Компания Synlogic работает над инженерными E. coli для иммуноонкологии. В 2023 году команда из Фреда Хатчинсона описала новый метод исследования некротических ядер опухолей.
Реалистичный прогноз: 5–10 лет до первых клинических испытаний конкретно этой платформы. Но если доклиника покажет хорошие результаты, это может стать одним из самых значимых прорывов в онкологии XXI века.
135 лет назад Уильям Коли вводил бактерии в опухоли вслепую, надеясь на чудо. Теперь инженеры создают бактерии, которые сами решают, когда и где нанести удар. От отчаянного эксперимента одинокого хирурга — к программируемым живым лекарствам. Путь оказался долгим. Но, возможно, мы наконец видим его финальный отрезок.
Часто задаваемые вопросы
Что происходит с бактериями после уничтожения опухоли?
C. sporogenes — строгий анаэроб: он погибает в присутствии кислорода. Когда некротическое ядро опухоли разрушается и в зону проникает кровь с кислородом, бактерии должны погибнуть естественным путём. Однако исследователи рассматривают дополнительные «kill switch» системы — генетические выключатели, которые заставят бактерий самоуничтожиться по внешнему сигналу. Это ещё один уровень безопасности.
Может ли бактерия мутировать и стать опасной?
Теоретически — да, как любой организм. Но кворум-сенсинг добавляет слой защиты: даже если мутация изменит одну бактерию, ей нужна критическая масса «единомышленников» для активации опасных генов. Кроме того, инженеры планируют использовать ауксотрофные штаммы — бактерии, которые не могут синтезировать ключевые аминокислоты и погибают без искусственной подкормки.
Чем это отличается от иммунотерапии рака?
Иммунотерапия (например, checkpoint-ингибиторы) «разблокирует» собственную иммунную систему пациента для борьбы с раком. Но она плохо работает против солидных опухолей с некротическим ядром — иммунные клетки просто не могут туда добраться. Бактериальная терапия работает именно там, куда не проникают другие подходы. В идеале оба метода будут дополнять друг друга.
Когда это станет доступно пациентам?
Команда из Уотерлу находится на стадии in vitro — до клинических испытаний ещё 5–10 лет. Однако другие бактериальные терапии уже в клинике: C. novyi-NT проходит Фазу II испытаний (NCT03435952). Если платформа из Уотерлу покажет хорошие результаты на животных, процесс может ускориться.
Для каких видов рака это может подойти?
Теоретически — для любых солидных опухолей с выраженным некротическим ядром. Наиболее вероятные кандидаты: глиобластома (рак мозга), панкреатический рак, саркомы — опухоли, которые плохо поддаются стандартной терапии и часто имеют обширные бескислородные зоны. Жидкие опухоли (лейкемии, лимфомы) для этого подхода не подходят.
Источники
Оригинал
Связанные
Читайте также
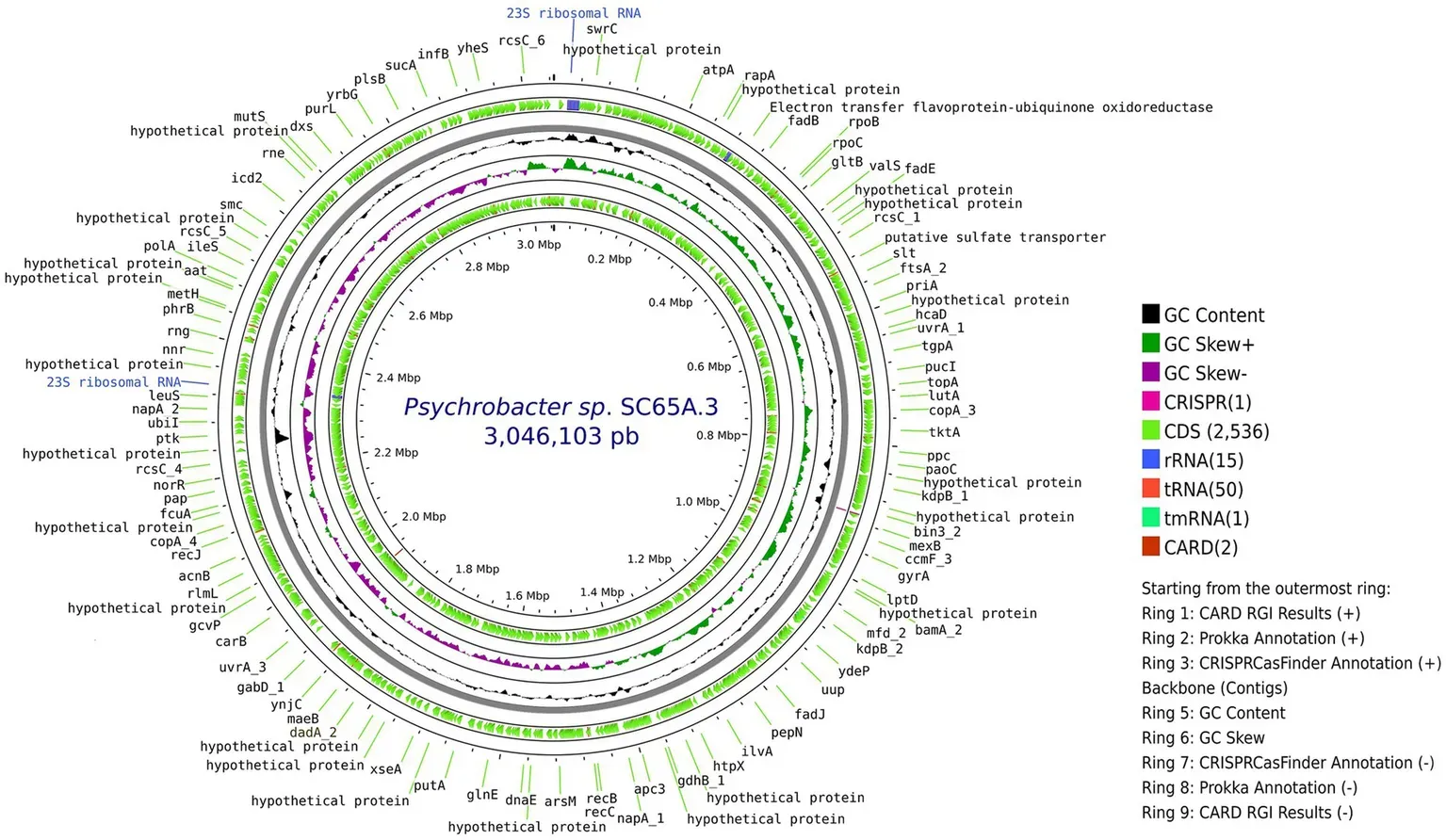
Бактерия из 5000-летнего льда устойчива к 10 антибиотикам — и может подсказать новые
В румынской пещере нашли микроб возрастом 5000 лет, устойчивый к 10 антибиотикам. Его гены — ключ к созданию новых лекарств.
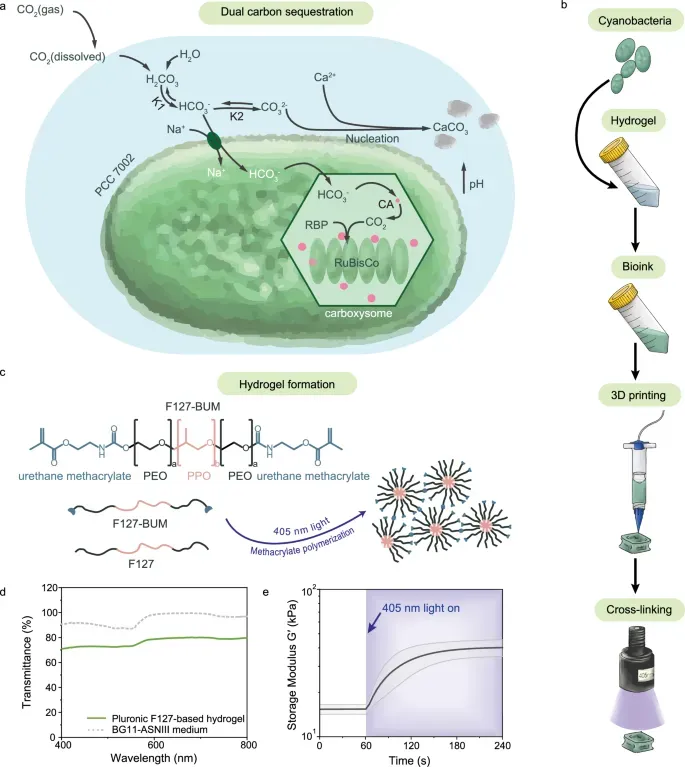
Живые здания: 3D-печатный гель с бактериями захватывает CO₂
Инженеры ETH Zurich создали 3D-печатный гидрогель с цианобактериями, который улавливает углекислый газ двумя путями — фотосинтезом и минерализацией карбонатов.
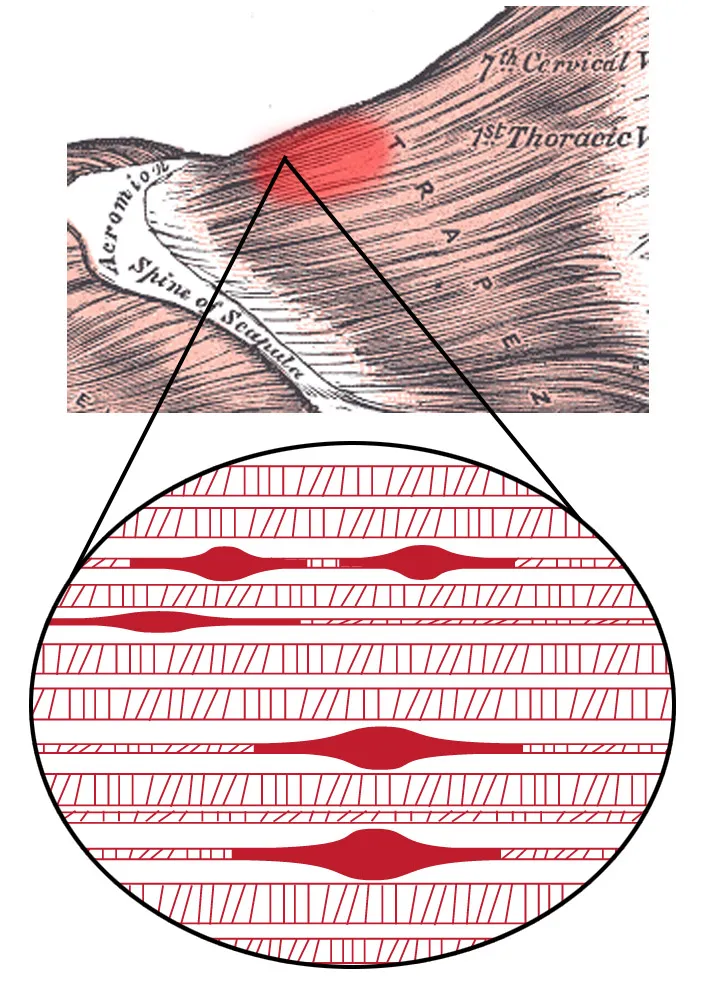
Мышечные узлы: что наука знает о триггерных точках и прорыв 2024 года
Почему в мышцах образуются болезненные уплотнения, чем они опасны и как от них избавиться — разбираем молекулярный механизм COL1A1/PDGFR-α, открытый в 2024 году.